3月18日,国家药监局药审中心发布《新生儿和低龄儿剂量推断技术指导原则》,帮助企业解决新生儿和低龄儿用药研发过程中面临的剂量选择难题,提高该人群药物研发效率,保障新生儿和低龄儿用药安全可及。
作为“十五五”规划开局之年,2026年我国儿童用药保障体系迎来系统性变革。今年1月,国务院公布的新版《中华人民共和国药品管理法实施条例》首次引入儿童用药品市场独占期制度,配合全国两会期间代表委员提出的多项专项议案,形成了从顶层设计到终端落地的政策闭环。
行业观点指出,这一制度创新与立法突破,正在破解长期困扰“用药靠掰、剂量靠猜”困境,标志着儿童用药保障进入全链条政策支持时代。
儿药研发技术规则持续完善
《新生儿和低龄儿剂量推断技术指导原则》适用于2岁及以下儿科人群药物研发过程中的剂量推断,旨在基于新生儿(包括早产儿)及低龄儿的生理、病理与发育药理学特征,在外推理论和临床开发策略基础之上,综合运用模型工具,提出剂量推断系统性方法,减少不必要的临床试验风险,提升新生儿和低龄儿药物开发的效率与可行性。
随着儿童用药研发的技术规则体系持续完善,我国儿童用药审评审批与上市进程也持续提速,政策红利加速落地。据国家药监局统计数据,截至2025年12月31日,本年度国家药监局共批准34个儿童用药,包括16个国产新药和18个进口新药;13个儿童用药通过优先审评审批程序批准上市,平均审评时间为305天,最快用时178天。
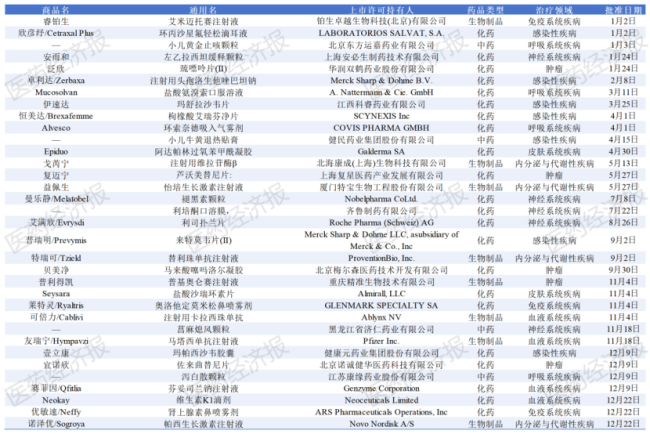
资料来源:国家药监局药审中心官网
其中多个1类新药获批上市,实现了相关用药的从无到有,如北海康成研发的注射用维拉苷酶β、复星医药研发的芦沃美替尼片和精准生物研发的普基奥仑赛注射液等。
此外,多个改良型新药获批上市,通过增加儿童适宜剂型,提高儿童服药依从性,促进药物的合理使用,如安必生研发的左乙拉西坦缓释颗粒、华润双鹤研发的巯嘌呤片(Ⅱ)和梅尔森医药研发的马来酸噻吗洛尔凝胶等。
今年全国两会期间,儿童用药保障也成为代表委员关注的焦点议题。全国政协委员丁列明提出建立儿童用药医保支付“专项通道”,建议对临床价值突出的儿童创新药实施“上市即谈判”机制,缩短从获批到医保准入的周期。
针对儿童药研发临床瓶颈,江苏省政协委员沈卫民提出构建“研-产-销”一体化激励机制,如对儿童药研发费用给予更高比例加计扣除,并将儿童药纳入集采单独分组。
研发投入持续加码
在政策红利与市场需求的双重驱动下,国内药企加速布局儿童用药领域。
上海复星医药在儿科用药领域进行了深度布局。在创新药物研发方面,芦沃美替尼片(FCN-159)作为MEK1/2选择性抑制剂,已获批用于治疗2岁及以上伴有症状、无法手术的丛状神经纤维瘤(NF1相关)儿童患者,以及朗格汉斯细胞组织细胞增生症(LCH)儿童患者。目前该药物在低级别脑胶质瘤等适应症上处于Ⅱ期临床试验阶段。
中药儿科龙头健民药业研发的小儿宣肺止咳颗粒新剂型、小儿牛黄退热贴膏相继获批。2025年上半年,其儿童药板块营收同比增长18%,大单品龙牡壮骨颗粒年销超12亿元。
头部企业的布局成效与业绩兑现,正是国内儿童用药市场持续扩容、结构优化的微观缩影。米内网数据显示,2025年中国儿童用药市场规模将突破2000亿元,年复合增长率12.8%。其中中成药市场规模预计达180亿元,占比38.5%;化学药占比52.7%;生物制品占比8.8%。抗感染药(29.3%)、呼吸系统用药(22.6%)和营养补充剂(18.9%)构成三大主力品类。值得关注的是,罕见病儿童用药成为新增长点,2025年市场规模突破65亿元,年增速达41%;随着市场独占期等政策落地,预计2026年儿童用药整体市场将突破2300亿元,创新剂型与专科药成为竞争焦点。
整体来看,从顶层制度设计的系统性完善,到审评审批体系的全链条优化,再到企业端研发投入的持续加码,我国儿童用药行业已进入政策驱动、创新引领、市场扩容的高质量发展新阶段,兼具临床价值、创新能力与产业化优势的药企,将在持续扩容的赛道中抢占先机。